EMA aprova vacina Spikevax para crianças dos 12 aos 17 anos
A Agência Europeia do Medicamento (EMA) deu “luz verde” à utilização da vacina da farmacêutica Moderna contra a COVID-19 na União Europeia (UE), para crianças dos 12 aos 17 anos, sendo o segundo fármaco contra a doença aprovado pelo regulador europeu para esta faixa etária.

SOCIEDADE E SAÚDE
COVID-19: VACINAÇÃO EM MARCHA
Embora com atrasos nas entregas por parte das empresas com quem a União Europeia (UE) negociou, em nome dos Estados-Membros, o último relatório de vacinação da Direção-Geral de Saúde (DGS), revela que já foram recebidas em Portugal 651 800 doses de vacinas contra a COVID-19 das quais foram distribuídas 571 981. LER MAIS
Em comunicado, a EMA informa que o seu comité de medicamentos humanos “recomendou a concessão de uma extensão de indicação para a vacina Spikevax COVID-19 [nome comercial da vacina da Moderna] para incluir a utilização em crianças com idades entre os 12 e os 17 anos”.
Esta vacina está já desde janeiro deste ano para adultos pelo regulador da UE e torna-se agora a segunda vacina anticovid-19 aprovada pela EMA para crianças dos 12 aos 17 anos, depois de a agência ter dado aval semelhante ao fármaco da [url-nolink=/pt/medicamentos/laboratorios/pfizer-biofarmaceutica-sociedade-unipessoal-lda/informacao-geral]Pfizer[/url]/BioNTech em maio passado.
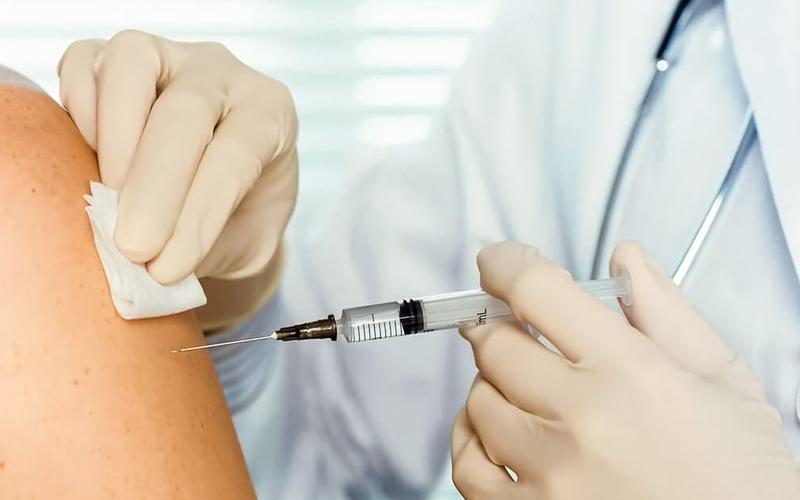
“A utilização da vacina Spikevax em crianças dos 12 aos 17 anos de idade será a mesma que em pessoas com 18 ou mais anos de idade. É administrada como duas injeções nos músculos da parte superior do braço, com quatro semanas de intervalo”, esclarece a EMA.
O regulador europeu indica ainda que “os efeitos da Spikevax foram investigados num estudo envolvendo 3 732 crianças dos 12 aos 17 anos de idade”, que revelou que esta vacina “produziu uma resposta de anticorpos comparável […] à observada em adultos jovens dos 18 aos 25 anos”.